
L’huile de CBD ne parvient pas à améliorer le contrôle des symptômes du cancer avancé
Avec autant d’articles dans les archives et plus d’une décennie d’écriture à laquelle se référer, il est fascinant de revenir sur la façon dont les contributeurs de ce blog ont examiné les problèmes médicaux émergents. Au cours de la même période de la vie de ce blog, la disponibilité de la marijuana à usage médical s’est considérablement élargie, ouvrant la voie à une éventuelle légalisation. Même très tôt, ce blog s’est montré prudent face au battage médiatique autour de son potentiel médical. Le premier article que j’ai pu trouver date de 2009, lorsque Peter Lipson a écrit sur son utilisation émergente. Il a noté:
Alors que la marijuana devient de plus en plus disponible à des fins médicales, les praticiens de la médecine scientifique doivent évaluer les preuves de l’utilisation de cette drogue. Lors de l’évaluation d’un nouveau médicament, nous devons nous poser un certain nombre de questions, notamment celles de l’innocuité, de l’efficacité et peut-être de la redondance. Les allégations d’efficacité de la marijuana ont tendance à être hyperboliques, aucune condition n’étant exemptée de ses avantages.
En 2014, David Gorski a écrit une série d’articles sur la marijuana médicale, la comparant à « la nouvelle herboristerie » et notant :
Il ne suffit pas de dire que le cannabis (ou tout autre cannabinoïde ou dérivé que vous souhaitez utiliser) est « efficace » contre cette maladie ou cette condition. Nous devons savoir à quel point il est efficace par rapport à la norme de soins existante.
L’enthousiasme du public pour l’usage récréatif et médical de la marijuana est clair. L’utilisation a augmenté de façon spectaculaire malgré des preuves limitées. Nous avons maintenant une étude qui aide à clarifier davantage son rôle potentiel en tant que médicament. Dans un nouvel article publié dans le Journal of Clinical Oncology, les chercheurs ont étudié si le cannabidiol (CBD) améliorait le contrôle des symptômes chez les patients atteints d’un cancer avancé.
L’huile de cannabidiol (CBD) est l’un des nombreux composés chimiques appelés cannabinoïdes qui sont isolés du cannabis. Le cannabis contient plus de 400 produits chimiques, dont au moins 120 cannabinoïdes, qui stimulent les récepteurs cannabinoïdes dans le corps. (Oui, nous avons des récepteurs cannabinoïdes et nous produisons même nos propres cannabinoïdes.) Les cannabinoïdes les plus étudiés dans le cadre de la recherche sont le delta-9-tétrahydrocannabinol (THC) et le CBD. Le CBD n’a pas le profil psychoactif du THC, et bien qu’il ait suscité un intérêt médical considérable, son rôle principal établi en tant que produit médical est le traitement des formes d’épilepsie infantile.
Le cannabidiol est un traitement plausible et même prometteur pour les symptômes du cancer avancé. Les patients atteints de cancer à un stade avancé peuvent éprouver de la fatigue, de l’anorexie et d’autres symptômes pénibles. Le cannabis a été promu comme une option de traitement plus « naturelle », cette étude a donc été conçue pour évaluer si l’huile de CBD, en combinaison avec des soins palliatifs standard, réduisait le fardeau des symptômes du patient.
Sommaire
Le procès
L’étude, intitulée « Phase IIb Randomized, Placebo-Controlled, Dose-Escalating, Double-Blind Study of Cannabidiol Oil for the Relief of Symptoms in Advanced Cancer (MedCan1-CBD) », était une étude randomisée et contrôlée par placebo du CBD qui a eu lieu dans cinq centres médicaux du Queensland, en Australie. Les participants avaient un cancer avancé (palliatif) et étaient âgés de plus de 18 ans avec des symptômes causant de la détresse (mesurés par un outil de notation standardisé), n’avaient pas de THC dans leur urine et avaient une mobilité (état de performance) et une fonction cognitive adéquates.
Tous les patients de l’étude devaient recevoir un traitement de soins palliatifs standard. Les patients ont été randomisés pour recevoir de l’huile de CBD (100 mg/mL) ou un placebo correspondant. Les doses ont été augmentées progressivement tous les trois jours, car ils pouvaient tolérer, sur 14 jours, à partir de 50 mg une fois par jour jusqu’à un maximum de 200 mg trois fois par jour. Les patients avaient la possibilité de rester sur la dose souhaitée pendant deux semaines supplémentaires.
Les patients ont été évalués par téléphone à l’aide d’un instrument standardisé (évaluation de la douleur, de la fatigue, des nausées, de la somnolence, de l’essoufflement, de l’appétit, de l’anxiété, de la dépression et du bien-être général) tous les 3 à 4 jours, avec des évaluations en face à face au jour 14 et 28. Ce score, au jour 14 par rapport au jour zéro, était la principale mesure de résultat. Les mesures secondaires comprenaient les scores de symptômes individuels, le contrôle de la douleur (mesuré par les équivalents de morphine orale) et les événements indésirables.
Résultats
Sur 215 patients invités à participer, 144 participants ont finalement été répartis au hasard sur une période de 33 mois. Deux patients ont finalement été retirés, ce qui a conduit à 58 participants sous CBD et 63 sous placebo comparable. Les groupes étaient comparables en termes de nombre de patients restés dans l’étude au jour 14 et au jour 28. Les caractéristiques des patients étaient comparables à l’exception du groupe placebo ayant un score de symptômes de base pire lors de la randomisation.
Charge totale des symptômes : les symptômes se sont améliorés dans les deux groupes sans différences significatives entre les deux groupes. (Les symptômes se sont en fait améliorés davantage dans le groupe placebo, mais pas de manière significative). Ajusté pour la différence dans le score de base, il n’y avait pratiquement aucune différence entre les deux groupes au jour 14. Il n’y avait pas non plus de différence dans la proportion de « répondeurs », définie comme une diminution de l’échelle des symptômes de six ou plus :
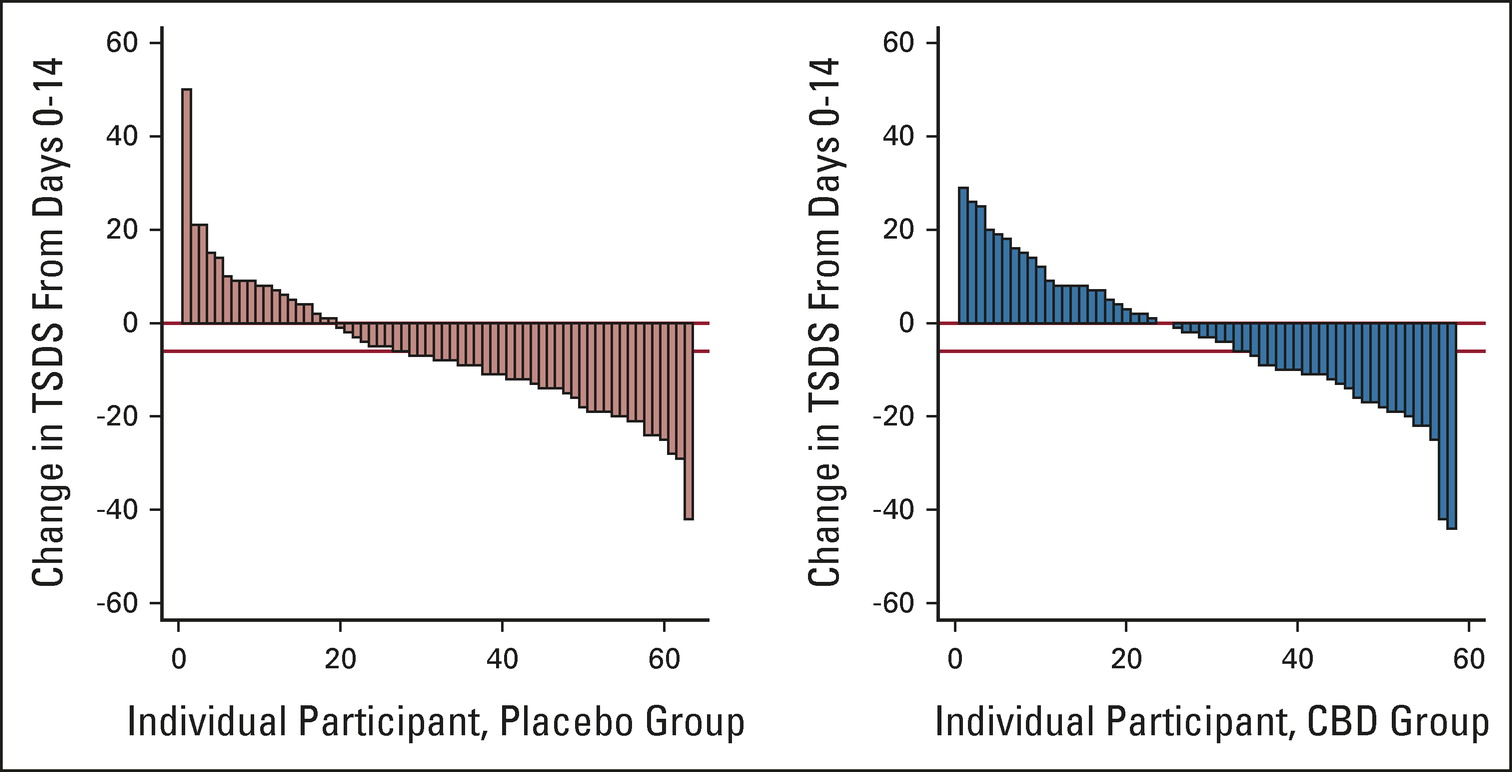
Proportion de répondeurs (diminution du score total de détresse des symptômes (TSDS) ≥ 6 entre le départ et le jour 14) dans chaque bras (placebo : 37 sur 63 [58.7%]; CDB : 26 sur 58 [44.8%]P = 0,13)
Modification des symptômes individuels : toutes les mesures de l’échelle des symptômes se sont améliorées (diminuées) au fil du temps dans les deux groupes. Il n’y avait aucune différence entre les groupes en termes de bien-être physique, émotionnel ou de bien-être, ni dans aucun élément individuel (par exemple, douleur, nausée, appétit) :
Dose sélectionnée par les participants : La dose finale médiane sélectionnée par les participants était de 6 ml/jour dans le groupe placebo et de 4 ml/jour dans le groupe CBD (équivalent à une dose de 400 mg/jour).
Contrôle de la douleur : Aucune différence n’a été détectée entre les bras en termes d’équivalents de morphine orale utilisés ou de changements d’utilisation sur la durée de l’étude.
Autres médicaments : Il n’y avait aucune corrélation entre la dose de CBD/placebo sélectionnée par le participant et la dose d’opioïdes, ou l’utilisation de médicaments comme les benziodiazépines et les antipsychotiques.
Impressions globales de changement : la plupart des participants ont déclaré se sentir mieux ou beaucoup mieux aux jours 14 et 28, souvent malgré l’absence de changement dans le score des symptômes. Il n’y avait pas de différences entre les groupes.
Effets indésirables : Il n’y a pas eu de différence d’événements d’intérêt particulier entre les groupes aux jours 14 et 28 en termes d’événements indésirables, avec une augmentation non significative de la somnolence et des douleurs abdominales et une tendance à plus de vomissements dans le groupe placebo. En termes d’autres événements indésirables, une augmentation significative de l’essoufflement a été signalée dans le groupe CBD. Il n’y avait aucune différence dans les hospitalisations (aucune liée au médicament à l’étude) ou dans la survie globale.
Conclusion
Bien qu’il y ait eu un enthousiasme considérable pour l’utilisation du cannabis en tant que traitement médical, cet essai contrôlé randomisé d’huile de CBD chez des patients n’a trouvé aucun avantage par rapport aux soins standard. Malgré un mécanisme d’action plausible, le CBD n’a pas amélioré de manière substantielle l’anxiété, la dépression ou tout autre symptôme individuel. L’huile de CBD était bien tolérée et il y avait peu d’effets secondaires avec le taux de somnolence plus élevé possible lié à l’utilisation de CBD.
Cet essai diffère des autres recherches en ce qu’il a été bien conçu pour minimiser les biais, a utilisé un produit CBD standardisé et vérifié, et a été conçu pour détecter si le CBD offrait des avantages significatifs. Il a mesuré les effets à l’aide d’une échelle validée qui capture les symptômes significatifs des patients. Les auteurs concluent :
Cette étude a des implications importantes pour les décideurs en ce qui concerne à la fois les indications approuvées de MC et son utilisation en toute sécurité. Le cannabis médical a été approuvé dans plusieurs pays pour les soins palliatifs dans l’idée qu’il pourrait améliorer la [quality of life] des patients atteints d’une maladie avancée. Le CBD est un produit à base de cannabis populaire dans la communauté car il n’a pas d’effets psychoactifs et n’altère pas la capacité de conduire. Avec les preuves actuelles, il est difficile de justifier la subvention gouvernementale du coût du CBD ni de recommander aux patients de payer pour les produits CBD.
Bien qu’aucune étude ne soit définitive, cet essai suggère que le CBD, malgré sa popularité, pourrait n’offrir aucun avantage aux patients gérant les symptômes d’un cancer avancé dans un cadre palliatif.
Afficher tous les articles
